FDA
Mallinckrodt的STRATAGRAFT®获FDA批准上市
6月15日,MallinckrodtPharmaceuticals plc的StrataGraft®获FDA批准,用于治疗成人患者的热烧伤(含有完整的真皮成分且适用于手术治疗)。该申请曾获得FDA孤儿药、再生医疗先进疗法和优先审评认定。
👇 点击查看:
Blueprint Medicines的AYVAKIT™获FDA批准上市
6月16日,Blueprint Medicines Corp.的Ayvakit™(avapritinib)获FDA批准,用于治疗成人患者的晚期系统性肥大细胞增多症(AdvSM),包括侵袭性系统性肥大细胞增多症(ASM)、伴随有一种血液瘤的系统性肥大细胞增多症(SM-AHN)以及肥大细胞白血病(MCL)。该申请曾获得FDA孤儿药、突破性治疗以及优先审评认定。

👇 点击查看:
United Therapeutics的TYVASO DPI™获FDA优先审评认定
6月16日,United TherapeuticsCorporation的Tyvaso DPI™ (inhaledtreprostinil) 获FDA优先审评认定,用于治疗肺动脉高压(PAH)以及间质性肺病相关的肺高压(PH-ILD)。

👇 点击查看:
NMPA
国家药品监督管理局批准利司扑兰口服溶液用散上市
近日,国家药品监督管理局通过优先审评审批程序批准罗氏制药公司申报的1类创新药利司扑兰口服溶液用散(商品名:艾满欣)上市,该品种为儿童罕见病治疗药品,适应症为2月龄及以上患者的脊髓性肌萎缩症(SMA)。
👇 点击查看:
https://www.nmpa.gov.cn/yaowen/ypjgyw/20210617084152178.html
国家药监局批准海曲泊帕乙醇胺片上市
近日,国家药品监督管理局通过优先审评审批程序批准江苏恒瑞医药股份有限公司申报的1类创新药海曲泊帕乙醇胺片(商品名:恒曲)上市,用于因血小板减少和临床条件导致出血风险增加的既往对糖皮质激素、免疫球蛋白等治疗反应不佳的慢性原发免疫性血小板减少症(ITP)成人患者,以及对免疫抑制治疗疗效不佳的重型再生障碍性贫血(SAA)成人患者。其中SAA适应症为附条件批准。
👇 点击查看:
https://www.nmpa.gov.cn/yaowen/ypjgyw/20210617084238109.html
勃林格殷格翰BI655130注射液纳入拟突破性治疗品种
近日,CDE信息公示,勃林格殷格翰(中国)投资有限公司的BI655130注射液纳入拟突破性治疗品种,拟用于治疗泛发性脓疱型银屑病(GPP)。
👇 点击查看:
http://www.cde.org.cn/news.do?method=changePage&pageName=service&frameStr=20#
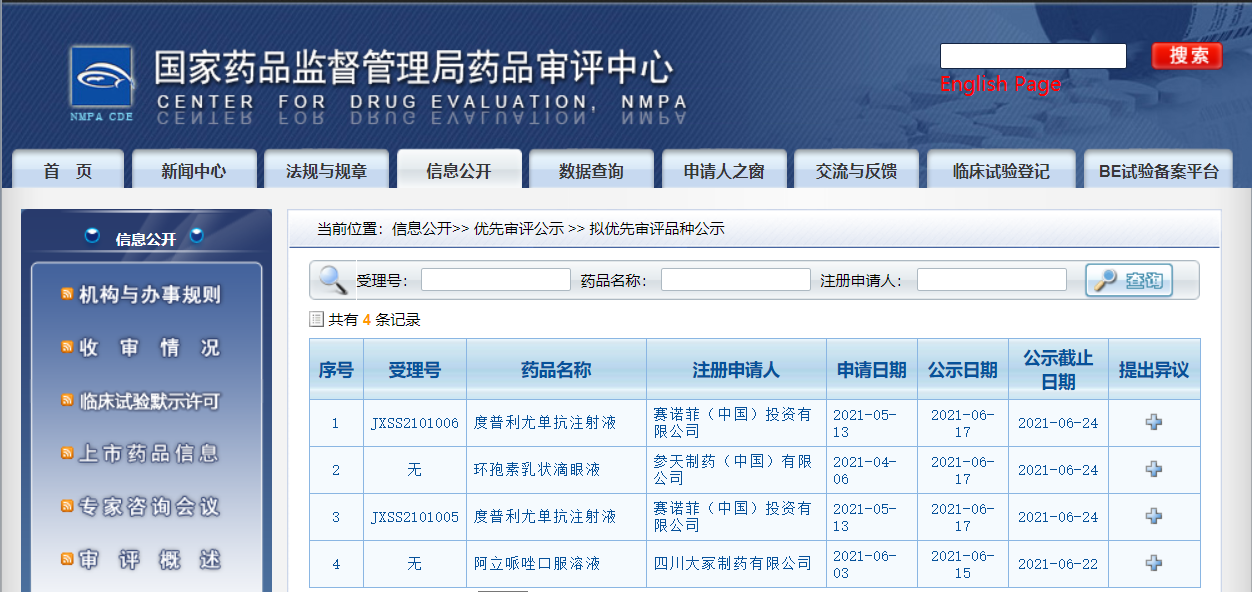
三款药物纳入拟优先审评品种
近日,CDE信息公示,三款药物纳入拟优先审评品种:
1. 四川大冢制药有限公司的阿立哌唑口服溶液,拟用于治疗6~17岁儿童和青少年的孤独症易激惹症状和抽动秽语综合征;
2. 赛诺菲(中国)投资有限公司的度普利尤单抗注射液(规格:200 mg/支和300 mg/支),拟用于治疗外用处方药控制不佳或不建议使用外用处方药的≥6岁至<12岁儿童和成人中重度特应性皮炎;
3. 参天制药(中国)有限公司的环孢素乳状滴眼液,拟用于治疗4岁及以上儿童和青少年的严重性春季角结膜炎。
👇 点击查看:
http://www.cde.org.cn/news.do?method=changePage&pageName=service&frameStr=20#


