奥来恩编者按
美国约有超10,000种罕见病影响着3000万人群,但其中90%的罕见病尚无FDA批准的治疗方法。由于罕见病的临床异质性高、患者基数小且机制研究有限等原因,罕见病药物研发面临诸多挑战。2023年9月,FDA发布了《基于一项充分且良好对照的临床试验联合确证性证据可作为有效性的实质性证据》指南草案,明确指出:在特定情况下,单项充分且良好对照(Adequate and Well-Controlled,AWC)临床试验加上确证性证据(Confirmatory Evidence,CE)就足以构成有效性的实质性证据(Substantial Evidence of Effectiveness,SEE),即可支持药品上市申请。详见《奥来恩药政前沿》第32期。
一般来说,新分子实体(New Molecular Entity,NME)的上市批准常需要开展两项或更多AWC临床试验,以证明其有效性与安全性。然而,对于患者招募困难、临床研究挑战较大的非肿瘤罕见病药物,监管机构(如FDA)也接受单项AWC试验加上CE的模式支持上市申请。在一项基于FDA批准新药数据的回顾性研究中,研究人员通过FDA内部数据库,分析了2020-2023年FDA批准的60项非肿瘤罕见病新药申请(NDA)和生物制品许可申请(BLA),探讨其有效性证据的构成模式和确证性证据来源,并与同期获批的非肿瘤一般性疾病NME进行比较。分析结果显示,在非肿瘤罕见病领域,67%(40种)治疗性NME基于单项AWC试验+CE的组合策略获批上市,成为主流监管决策模式;另有20%(12种)使用了单项具有高度说服力的AWC试验以说明“SSE”支持批准(见图1)。相比之下,同期(2020-2023年)获批上市的非肿瘤一般性疾病的NME中,仅29%(20/69)采用单项AWC+CE或单项AWC策略,而其余71%(49/69)仍遵循传统的两项或更多AWC试验要求。这一差异表明,罕见病药物在临床证据要求上具有更高的灵活性,对“单项AWC试验+CE的组合”提供SEE支持批准的依赖明显更高。
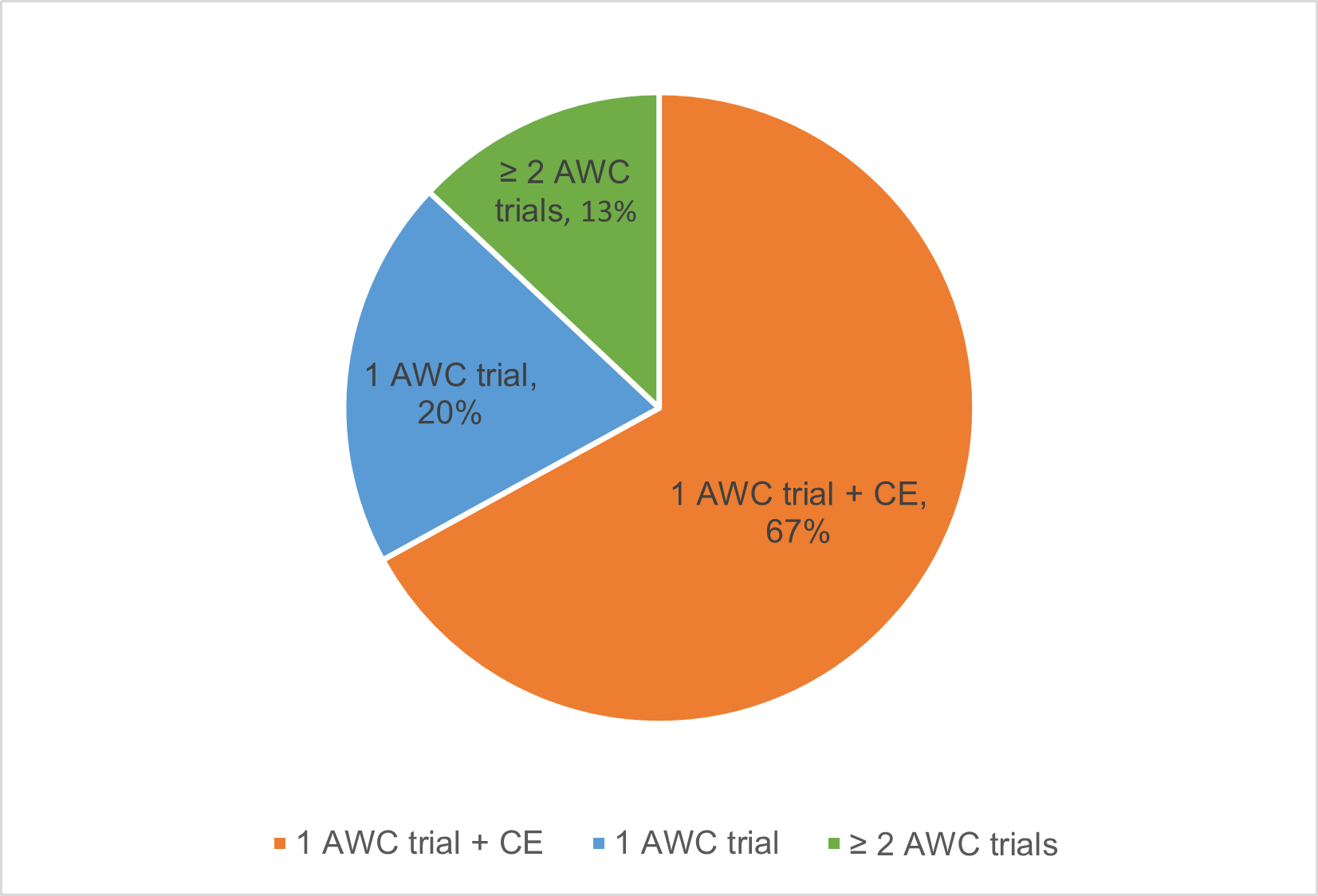
图1. 2020-2023年FDA批准的非肿瘤罕见病NME确立有效性的实质性证据(SEE)的依据(AWC与CE占比)
确证性证据类型解读与建议:
在上述40项采用AWC+CE策略的申请中,最常见的确证性证据类型是机制或药效学证据,占比高达77.5%;其他CE类型包括相关动物模型证据、相同药理学分类的其他产品的证据(如同靶点类似产品的交叉外推数据)、自然病史证据等。此外,还有部分申请同时使用多种类型的确证性证据或未归类的证据,增强说服力。作为确证性证据的机制或药效学证据通常由药效学生物标志物、作用机制验证研究组成。
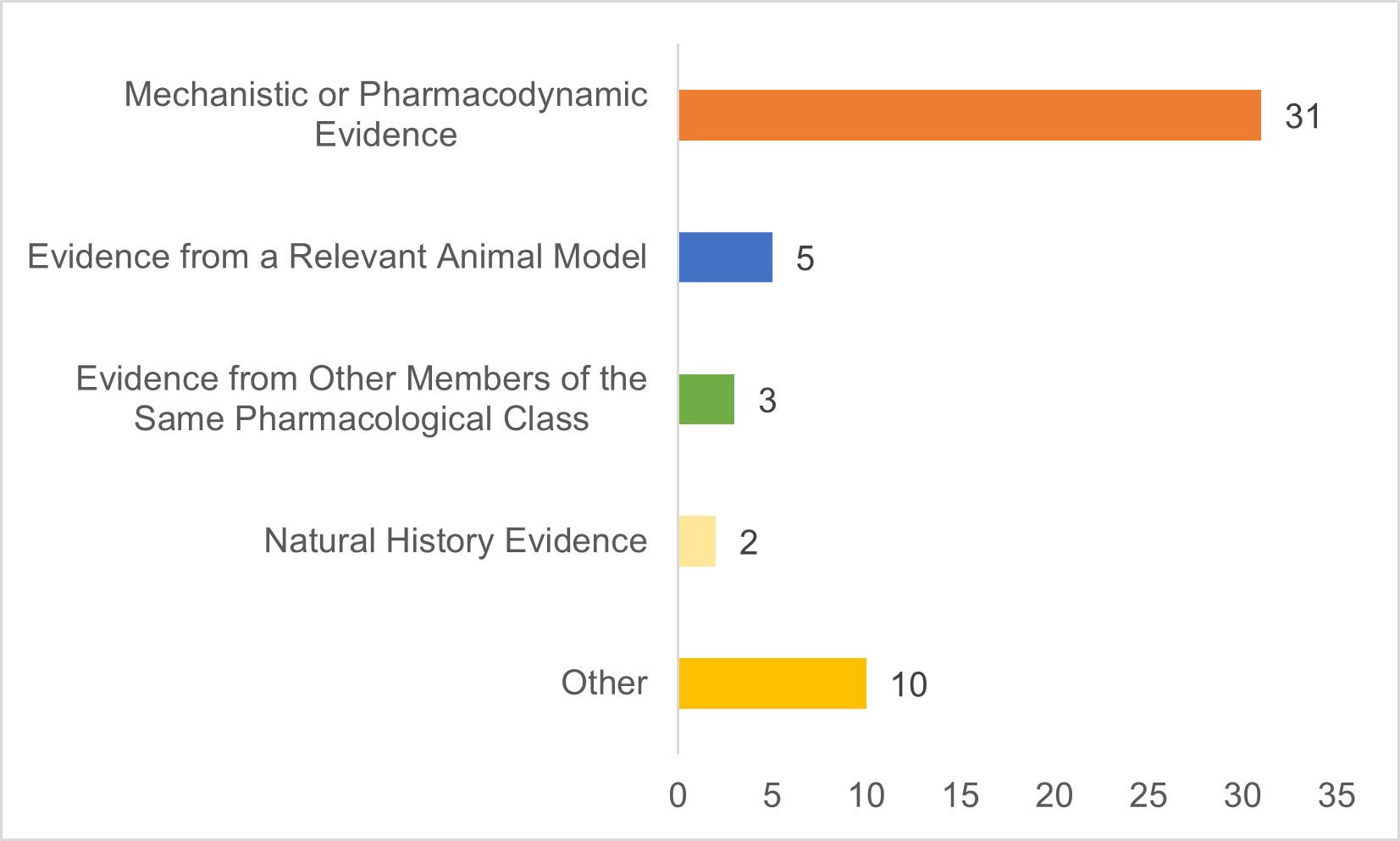
图2. 2020-2023年FDA批准的非肿瘤罕见病NME所用的确证性证据类别
成功示例:Avalglucosidase alfa-ngpt、Fosdenopterin与Leniolisib
这三款获批产品均基于1项AWC试验加CE支持上市,其中CE类型包括机制证据、动物模型和药效学证据、药代动力学/暴露-效应数据等,表明科学合理的证据组合可有效满足监管对有效性的实质性证据的要求。
奥来恩建议:
罕见病药物的临床研究面临诸多挑战,前瞻性思考确证性证据在加快罕见病药物研发中至关重要。随着FDA在罕见病领域监管思路的动态调整,结合奥来恩多年的实操经验,我们提出以下建议:
-
在研发早期即评估是否具备采用AWC+CE的可行性;
-
明确可能可用的确证性证据类型,并尽早开展机制研究或生物标志物验证;
-
主动与FDA沟通与交流,借助合适的会议类型,如Type B pre-IND会议、EOP会议、Type C或D会议等,就拟采用的策略与证据类型提前达成一致。
奥来恩将会为您带来FDA及其他监管机构更多药政法规动态,欢迎大家订阅《奥来恩药政前沿》。大家对本期主题感兴趣可以在评论区提问并讨论,评论热度最高的送出精美礼品,并且抽1个转发送礼品,欢迎大家积极讨论与转发。若您有任何问题欢迎与奥来恩咨询与交流!(邮箱:bd@aleonpharma.com;手机:17761872613)。


