奥来恩编者按
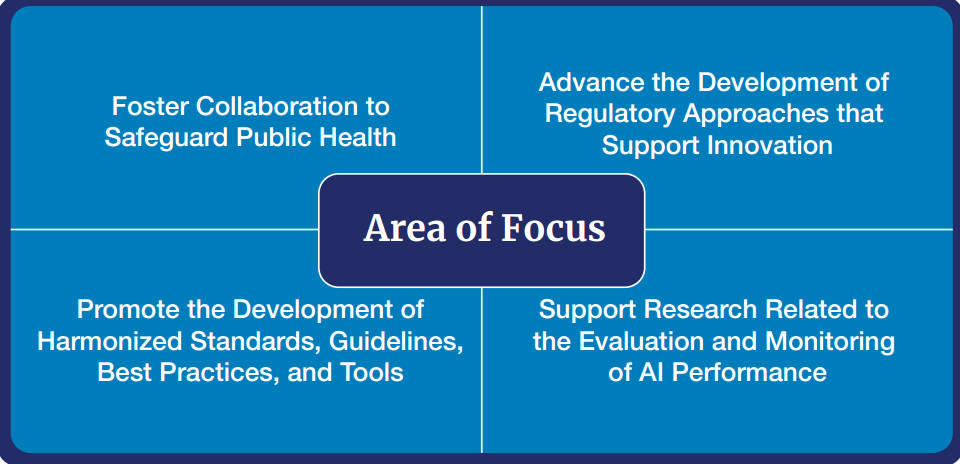
人工智能(Artificial Intelligence,AI)的开发、部署、使用与维护所涉及的复杂动态的过程受益于整个医疗产品生命周期的精心管理。3月15日,FDA发表了新论文《人工智能与医疗产品:CBER、CDER、CDRH和OCP如何协同工作》,该论文概述了FDA生物制品评估与研究中心(Center for Biologics Evaluation and Research,CBER)、药物评价与研究中心(Center for Drug Evaluation and Research,CDER)、器械和放射健康中心(Center for Devices and Radiological Health,CDRH)和组合产品办公室(Office of Combination Products,OCP)在整个医疗产品生命周期中开发和使用AI的四个重点区域。
FDA医疗产品中心与研发人员、患者团体、学术界、全球监管机构和其他利益相关方密切合作,发展以患者为中心的监管方法,该机构计划:
2.促进教育举措的制定,来支持在医疗产品生命周期中安全负责地使用AI;
3.继续与全球合作者密切合作。
FDA医疗产品中心计划制定政策,为AI的使用提供监管可预测性和明确性,该机构计划:
2.开发评估AI算法的方法,以评估并监管AI在医疗产品生命周期中的使用;
3.利用并继续扩大现有举措;
4.发布关于在医疗产品生命周期中使用AI的指南。
FDA医疗产品中心致力于维护AI医疗产品的安全性与有效性标准,该机构计划:
2.确定并促进对AI医疗产品进行长期安全和实际性能监测的最佳实践;
3.探索关于记录和确保用于训练和测试AI模型的数据符合使用要求的最佳方法,包括充分代表人群;
4.为医疗产品生命周期中使用的AI工具或系统制定质量保证的框架与战略。
为了深入了解AI对医疗产品安全性和有效性的影响,在现有资源的情况下,中心支持以下示范项目:
2.支持考虑到在医疗产品开发中使用AI相关的健康不平等的项目,以促进公平并确保数据代表性;
3.支持将持续监测医疗产品开发中的AI工具的项目,以确保遵守标准,并在整个生命周期内保持性能和可靠性。
FDA制定本文件是为了促进以负责任和符合伦理的方式开发、部署、使用和维护使用AI的医疗产品。FDA将保持与美国和全球各方接触的开放渠道。CBER、CDER、CDRH和OCP计划调整AI在医疗产品中使用的监管方法,以保护患者和医护人员,并以促进创新的方式确保医疗产品的网络安全(Cybersecurity)。
奥来恩将会为您带来FDA及其他监管机构更多药政法规动态,欢迎大家订阅《奥来恩药政前沿》。大家对本期主题感兴趣可以在评论区提问并讨论,评论热度最高的送出精美礼品,并且抽1个转发送礼品,欢迎大家积极讨论与转发。若您有任何问题欢迎与奥来恩咨询与交流(邮箱:bd@aleonpharma.com;手机:17761872613)。


