第8期 / 本文由奥来恩团队原创
奥来恩编者按:
“中国的生物制药到2028年可能会对全球制药行业产生更大影响,但药政发展和国际合作的质量将决定该行业如何发展。”
中美双报_FDA IND/NDA/BLA_新药注册-奥来恩医药
自2015年以来,中国生物制药行业蓬勃发展,在全球制药生态系统中逐渐崭露头角。药政监管体系的改革、活跃的资本市场、以及逐步完善的创新环境,无不推动着中国生物制药行业的快速前进。中国生物医药行业,正在潜移默化对全球生物制药行业的发展产生影响,而不再只是关于中国的故事 。今年8月,麦肯锡公司(McKinsey & Company)发布了题为《Vision2028: How China could impact the global biopharma industry》的报告。该报告描述了中国生物制药行业的发展现状,指出影响中国生物制药行业未来发展的重要因素,并预测了未来发展的三种不同情形、以及如何抓住中国制药行业发展的机会。
该报告通过调研,从3个方面共9个维度对中国生物制药行业发展的现状进行了分析(见图1)。这3个方面包括驱动力(Enablers)、价值链能力(Value Chain Capabilities)和创新(Innovation)。其中,每个方面又分别包括了3个维度,即:
1) 驱动力:药政监管发展与国际接轨(Regulatory Integration)、资金水平(Level of Funding)及跨境合作与交易(Cross-Border Tansactions)
2) 价值链能力:研究与发现(Research and Discovery)、临床开发(Clinical Development)及生产制造(Manufacturing)
3) 创新:负担得起的创新(Affordable Innovation)、突破性创新(Breakthrough Innovation)及技术创新(Enabling Technologies)

该报告在谈到决定未来五至十年中国对全球生物制药行业产生影响的四大关键因素中,首先对融入全球药政监管和卫生体系(Integrationinto global regulatory and health systems)进行了分析,认为这将成为中国制药企业“出海”的重要的一步。同时,面临诸多海外药政监管体系与机构,如何提供满足国际要求的临床数据、以及符合监管机构对数据严谨性和数据披露的要求、关注具体适应症标准治疗的变化等,对中国的创新药能否被海外药监机构和医保体系接受,将起到决定性作用。
在预测中国生物制药行业最有可能出现的持续增长情景(Continued Momentum)中,认为药政监管改革和融入全球监管系统将会继续,全球监管一体化将不会遇到重大障碍(见图2)。此外,面对目前仍然相对落后的临床开发现状,中国制药公司必须了解全球监管药政法规与政策,并在与其沟通中获得更多经验。例如,今年2月PD-1单抗被FDA拒绝批准,其主要原因是缺乏更能代表美国患者群体、并符合美国当前治疗标准的多区域临床试验(MRCT)数据。特别是FDA已明确表示,药物批准将会取决于多地区临床试验的数据。因此,中国药企需要做出重大改变,制定合理的临床开发策略,并培养能够应对药政监管机构对临床数据严格监管与审查的专业技能。
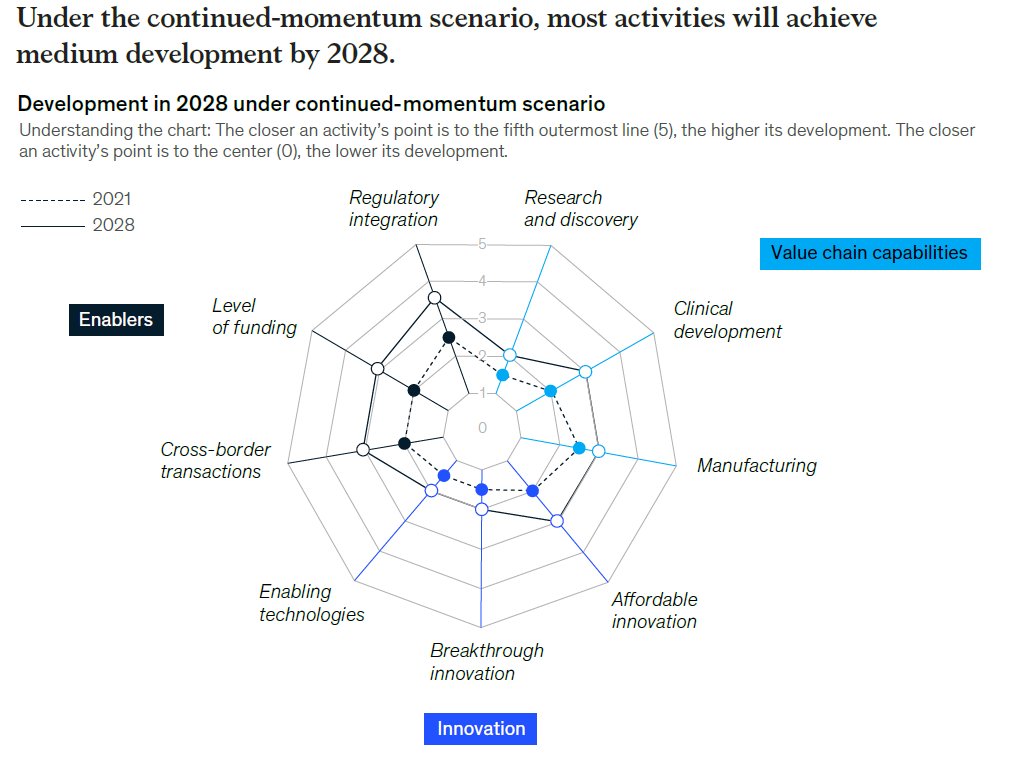
图2. 中国生物制药行业未来持续增长的情形 (来源:McKinsey&Company)
为了获得持续的发展并增加全球影响力,中国生物制药企业需要调整公司运营策略,将药物研发重点转移到未满足的医疗需求上,并不断寻求可行的全球化途径。我们坚信,到2028年,中国生物制药行业将拥有更多全球创新,为全世界患者带来更多获益。奥来恩作为全球药政法规与策略咨询公司,将会利用我们丰富的知识和经验帮助中国的生物制药企业在国际化的征程中走得更深更远。
点击查看:
[1]. McKinsey & Company. Vision 2028: How China could impact the global biopharma industry. August 2022.


