第49期 / 本文由奥来恩团队原创
本期看点:首个用于治疗幼儿COVID-19的药物获FDA批准;CDE发布《抗肿瘤药物说明书不良反应数据汇总指导原则》;多款药物获药监机构特殊审评认定。
中美双报_FDA IND/NDA/BLA_新药注册-奥来恩医药
重要会议
• FDA,2022.05.04-05.06,Getting the Dose Right: Optimizing DoseSelection Strategies in Oncology – An FDA-ASCO Virtual Workshop
COVID-19
【FDA】首个!用于治疗幼儿COVID-19的药物获FDA批准
近日,FDA扩大了COVID-19治疗药物Veklury(remdesivir)批准使用的人群,包括了年龄28天及以上(体重至少3公斤,约7磅)且SARS-CoV-2病毒直接检测结果阳性的儿童患者。这些患者需要具备以下条件:住院或不住院且患有轻至中度COVID-19、并存在高风险进展为重度COVID-19,包括住院和死亡。
来源:FDA官网
法规政策
【NMPA】CDE发布《抗肿瘤药物说明书不良反应数据汇总指导原则》
随着抗肿瘤药物研发的进展,越来越多的研究表明,一种药物可以应用于不同瘤种、同一瘤种的不同阶段或人群,还可以与不同作用机制的药物联合。在一种药物单用以及联合用药积累了大量的安全性数据的情况下,面对不同的使用者,如何科学、全面、清晰、简洁、易读地在说明书中呈现药物在不同使用场景下的安全性特征,切实保障患者用药安全,是目前监管方及业界亟需解决的问题。近日,CDE正式发布了《抗肿瘤药物说明书不良反应数据汇总指导原则》。
来源:CDE官网
点击查看:
https://www.cde.org.cn/main/news/viewInfoCommon/ba1a3e96f3ab0dc18a18416be7345f2f
特殊审评
【FDA】Tvardi Therapeutics的TTI-101获FDA孤儿药认定
近日,Tvardi Therapeutics, Inc.的TTI-101获FDA孤儿药认定(Orphan Drug Designation, ODD),用于治疗肝细胞癌(HCC)。TTI-101是一种靶向信号传导及转录激活蛋白(STAT)3的口服小分子抑制剂。
来源:businesswire官网
【FDA】康诺亚CMG901获FDA快速通道认定
近日,康诺亚CMG901获FDA快速通道认定(Fast Track Designation, FTD),用于治疗复发/难治性胃癌和胃食管结合部腺癌。CMG901是全球首个也是目前唯一获得FDA快速通道认定的Claudin 18.2靶点在研药物,且此前曾获得FDA孤儿药认定。

来源:康诺亚官网
点击查看:
https://www.keymedbio.com/show-132-194-1.html
【FDA】OncoC4的ONC-392获FDA快速通道认定
近日,OncoC4, Inc.的ONC-392获FDA快速通道认定,用于单药治疗此前接受抗PD-(L)1治疗后疾病进展的转移性非小细胞肺癌(NSCLC)患者。ONC-392是一种抗CTLA-4单克隆抗体,且保留了CTLA-4免疫检查点功能。

来源:ONCOC4官网
【FDA】VBL THERAPEUTICS的OFRA-VEC获FDA快速通道认定
近日,VBL Therapeutics的Ofra-vec(ofranergene obadenovec或者VB-111)与Paclitaxel联用获FDA快速通道认定,用于治疗铂耐药的卵巢癌。

来源:VBL THERAPEUTICS官网
【FDA】阿斯利康ENHERTU新适应症获FDA优先审评认定
近日,FDA接受了由阿斯利康和第一三共联合开发的Enhertu(trastuzumab deruxtecan)的补充生物制品许可申请(sBLA)并授予优先审评认定(Priority Review),用于治疗手术不可切除或转移性且肿瘤含HER2(ERBB2)变异的非小细胞肺癌(NSCLC)成人患者,这些患者曾接受过系统治疗。
来源:阿斯利康官网
【NMPA】艾力斯医药甲磺酸伏美替尼片纳入拟突破性治疗品种
近日,上海艾力斯医药科技股份有限公司的甲磺酸伏美替尼片纳入拟突破性治疗品种,拟用于经检测确认存在表皮生长因子受体(EGFR)20外显子插入突变阳性,含铂化疗期间或化疗后出现疾病进展的局部晚期或转移性非小细胞性肺癌(NSCLC)成人患者的治疗。
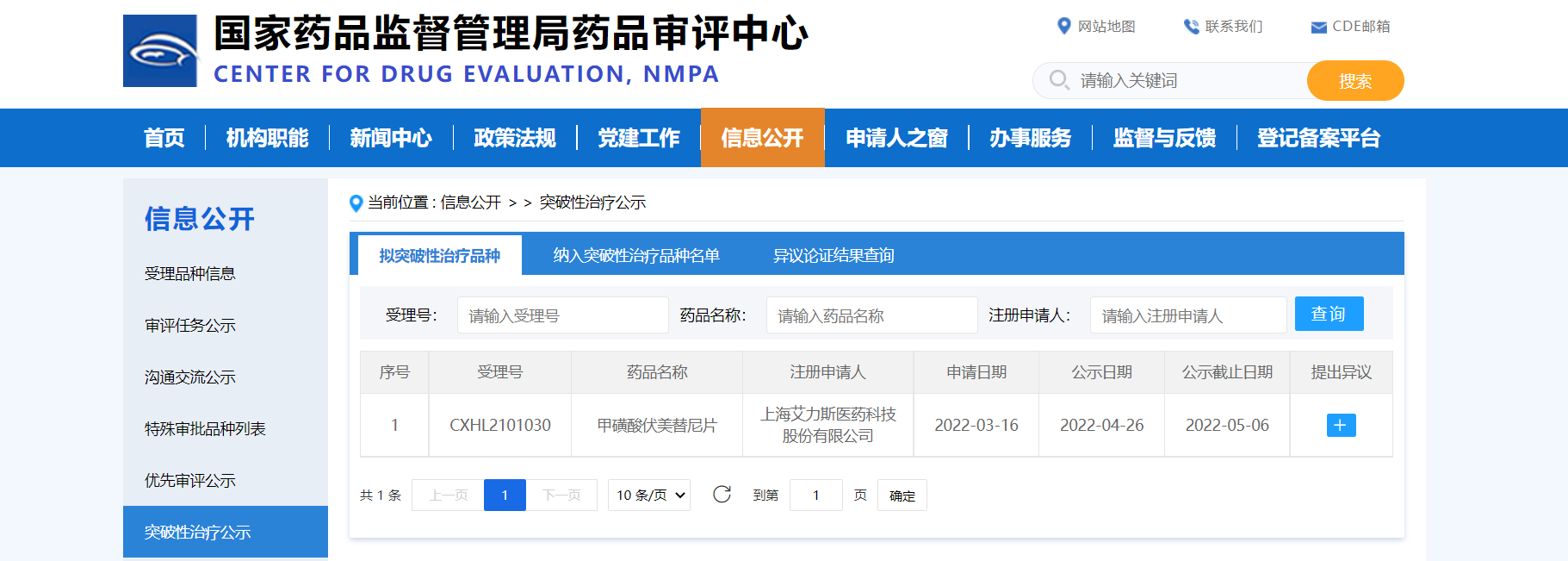
来源:CDE官网
点击查看:
https://www.cde.org.cn/main/xxgk/listpage/2f78f372d351c6851af7431c7710a731
【NMPA】两款药物纳入拟优先审评品种
近日,两款药物纳入拟优先审评品种:
1. 国药一心制药有限公司的注射用阿糖胞苷,拟用于成人和儿童急性非淋巴细胞性白血病的诱导缓解和维持治疗;
2. 第一三共(中国)投资有限公司的注射用Trastuzumab Deruxtecan,拟用于治疗既往接受过一种或一种以上抗HER2药物治疗的不可切除或转移性HER2阳性成人乳腺癌患者。
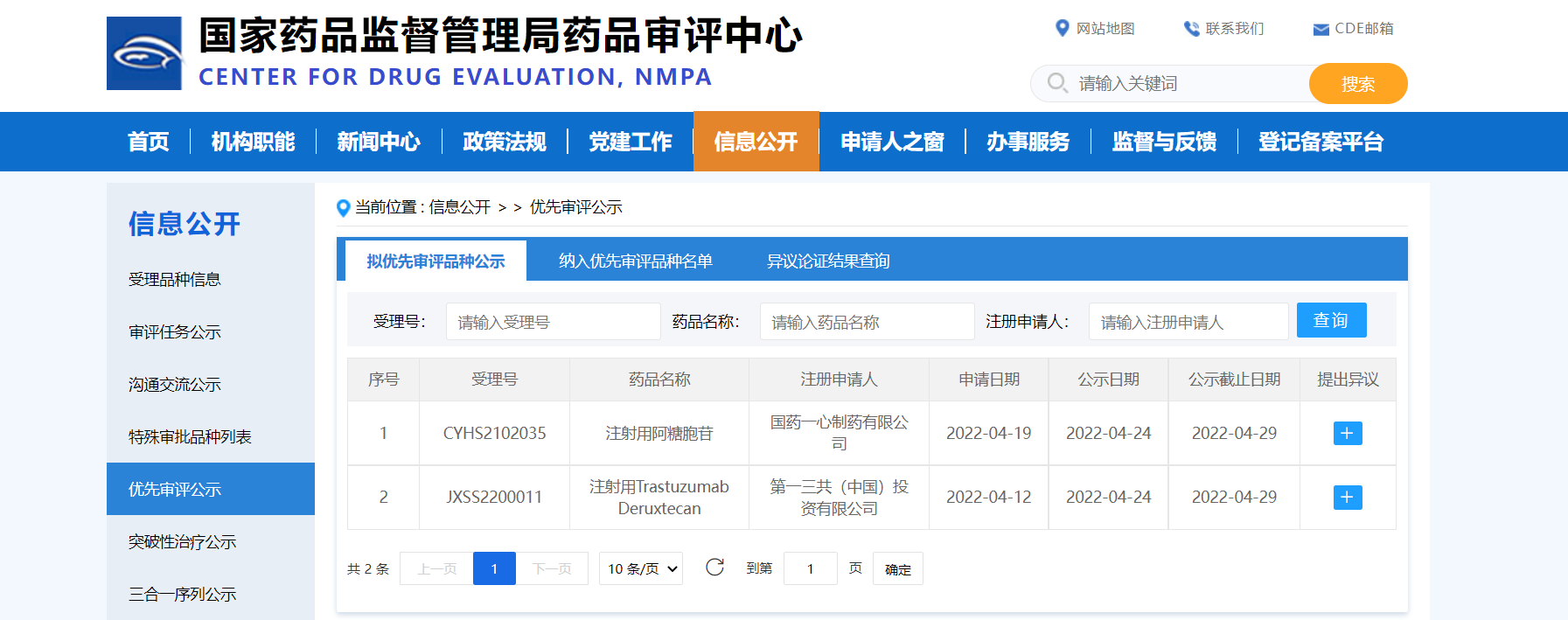
来源:CDE官网
点击查看:
https://www.cde.org.cn/main/xxgk/listpage/2f78f372d351c6851af7431c7710a731


