FDA
C4 Therapeutics的CFT7455获FDA孤儿药认定
8月11日,C4 Therapeutics,Inc.的CFT7455获FDA孤儿药认定,用于治疗多发性骨髓瘤。

来源:C4 Therapeutics官网
Vitality的VBX-100获FDA孤儿药认定
8月10日,Vitality Biopharma, Inc.的VBX-100获FDA孤儿药认定,用于治疗儿童溃疡性结肠炎。

来源:Vitality官网
点击查看:
https://vitality.bio/fda-grants-vitality-biopharma-orphan-drug-designation-for-vbx-100-prodrug/
Apexigen的APX005M获FDA孤儿药认定
8月5日,Apexigen, Inc.的APX005M(sotigalimab)获FDA孤儿药认定,用于治疗软组织肉瘤。

来源:Apexigen官网
点击查看:
https://www.apexigen.com/news/08-05-21/
PharmaTher的KETAMINE获FDA孤儿药认定
8月4日,PharmaTher Holdings Ltd.的Ketamine获FDA孤儿药认定,用于治疗肌萎缩侧索硬化(ALS)。
来源:PharmaTher官网
点击查看:
https://www.pharmather.com/news
中美双报、新药注册,尽在奥来恩!
Aldeyra Therapeutics的ADX-2191获FDA孤儿药认定
8月4日,Aldeyra Therapeutics, Inc.的ADX-2191获FDA孤儿药认定,用于治疗视网膜色素变性(RP)。

来源:Aldeyra官网
RELIEF THERAPEUTICS的RLF-100获FDA孤儿药认定
8月3日,RELIEF THERAPEUTICS Holding AG的RLF-100获FDA孤儿药认定,用于治疗结节病。

来源:Relief官网
Autobahn Therapeutics的ABX-002获FDA孤儿药认定
8月2日,Autobahn Therapeutics的ABX-002获FDA孤儿药认定,用于治疗X-连锁肾上腺脑白质营养不良(X-ALD)。

来源:Autobahn官网
Calliditas的SETANAXIB获FDA快速通道认定
8月9日,Calliditas Therapeutics AB的Setanaxib获FDA快速通道认定,用于治疗原发性胆汁性胆管炎(PBC)。

来源:Calliditas官网
Moderna的呼吸道合胞病毒mRNA疫苗获FDA快速通道认定
8月3日,Moderna, Inc.的呼吸道合胞病毒(RSV)疫苗(mRNA-1345)获FDA快速通道认定,用于60岁及以上人群呼吸道合胞病毒的预防。

来源:Moderna官网
Alkermes的NEMVALEUKIN获FDA快速通道认定
8月2日,Alkermes plc的Nemvaleukin Alfa (nemvaleukin) 获FDA快速通道认定,用于治疗黏膜黑色素瘤。

来源:Alkermes官网
Eiger的AVEXITIDE获FDA突破性治疗认定
8月5日,Eiger BioPharmaceuticals, Inc.的Avexitide获FDA突破性治疗认定,用于治疗先天性高胰岛素血症(HI)。

来源:Eiger官网
Merck的KEYTRUDA®补充生物制品许可申请获FDA优先审评认定
8月10日,Merck的KEYTRUDA®(pembrolizumab)补充生物制品许可申请获FDA优先审评认定,作为术后有复发风险(中至高或高风险)的肾细胞癌(RCC)患者的辅助治疗。

来源:Merck官网
Daré Bioscience的DARE-BV1获FDA优先审评认定
8月9日,Daré Bioscience, Inc.的DARE-BV1获FDA优先审评认定,用于治疗细菌性阴道病。

来源:Daré Bioscience官网
Exelixis的CABOMETYX®获FDA优先审评认定
8月5日,Exelixis, Inc.的Cabometyx®(cabozantinib)获FDA优先审评认定,用于治疗12岁及以上患者(接受先前的治疗后进展、且放射性碘难治)的分化型甲状腺癌(DTC)。
来源:Exelixis官网
Genentech的TECENTRIQ®获FDA优先审评认定
8月2日,Genentech的Tecentriq®(atezolizumab) 获FDA优先审评认定,作为肿瘤PD-L1表达大于等于1%的非小细胞肺癌患者(NSCLC)手术或者铂类化疗之后的辅助治疗。
来源:Genentech官网
点击查看:
https://www.gene.com/media/press-releases/14924/2021-08-02/fda-grants-priority-review-to-genentechs
NMPA
CDE正式发布《急性非静脉曲张性上消化道出血治疗药物临床试验技术指导原则》
8月5日,为进一步规范和指导急性非静脉曲张性上消化道出血治疗药物临床试验,提供可参考的技术规范,在国家药品监督管理局的部署下,CDE正式发布了《急性非静脉曲张性上消化道出血治疗药物临床试验技术指导原则》。

来源:CDE官网
点击查看:
http://www.cde.org.cn/news.do?method=viewInfoCommon&id=db64fe5936999ec5
两款药物纳入拟突破性治疗品种
近日,CDE信息公示,两款药物纳入拟突破性治疗品种:
1. 复星凯特生物科技有限公司的阿基仑赛注射液,拟用于治疗接受过二线或以上系统治疗后复发或难治性惰性非霍奇金淋巴瘤,包含滤泡性淋巴瘤(简称FL)和边缘区淋巴瘤(简称MZL);
2. 葛兰素史克(中国)投资有限公司的GSK3228836 注射液,拟用于治疗慢性乙型肝炎。
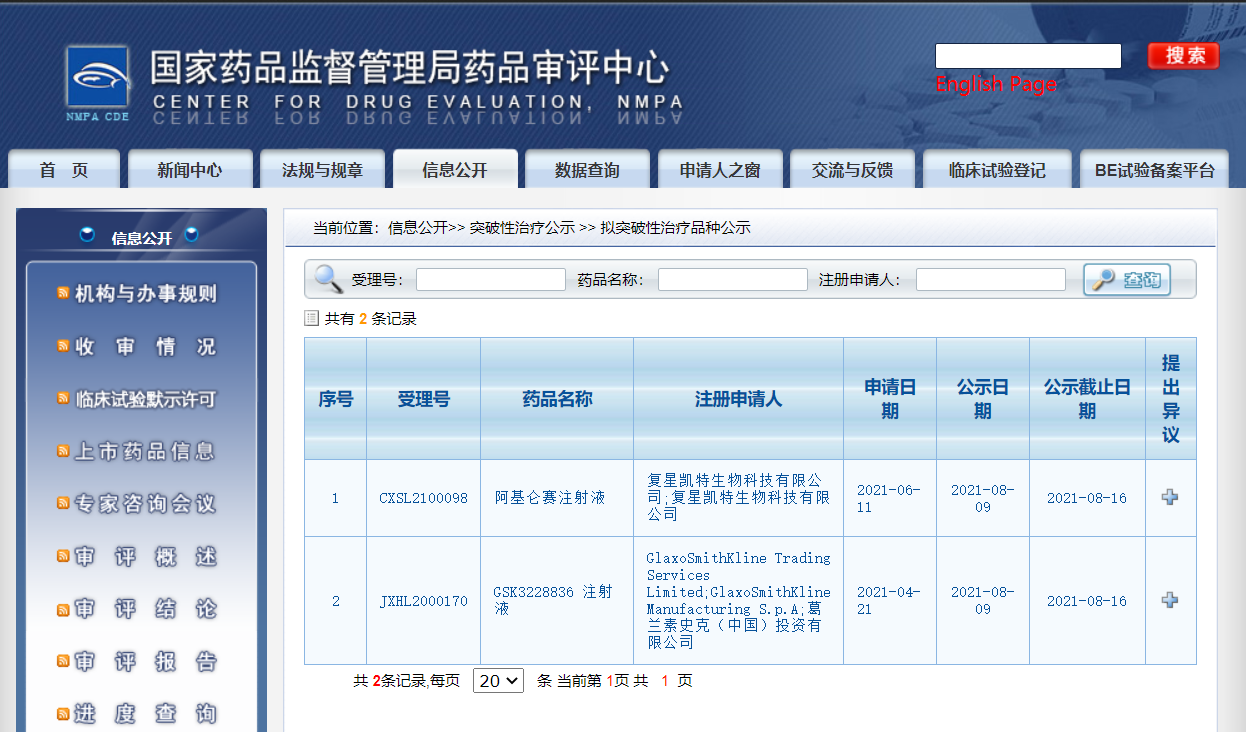
来源:CDE官网
点击查看:
http://www.cde.org.cn/news.do?method=changePage&pageName=service&frameStr=20#
泰格医药维托拉生注射液纳入拟优先审评品种
近日,CDE信息公示,杭州泰格医药科技股份有限公司的维托拉生注射液被纳入拟优先审评品种,拟用于治疗肌营养蛋白的基因缺失经验明可通过53号外显子跳跃治疗的杜氏肌营养不良。
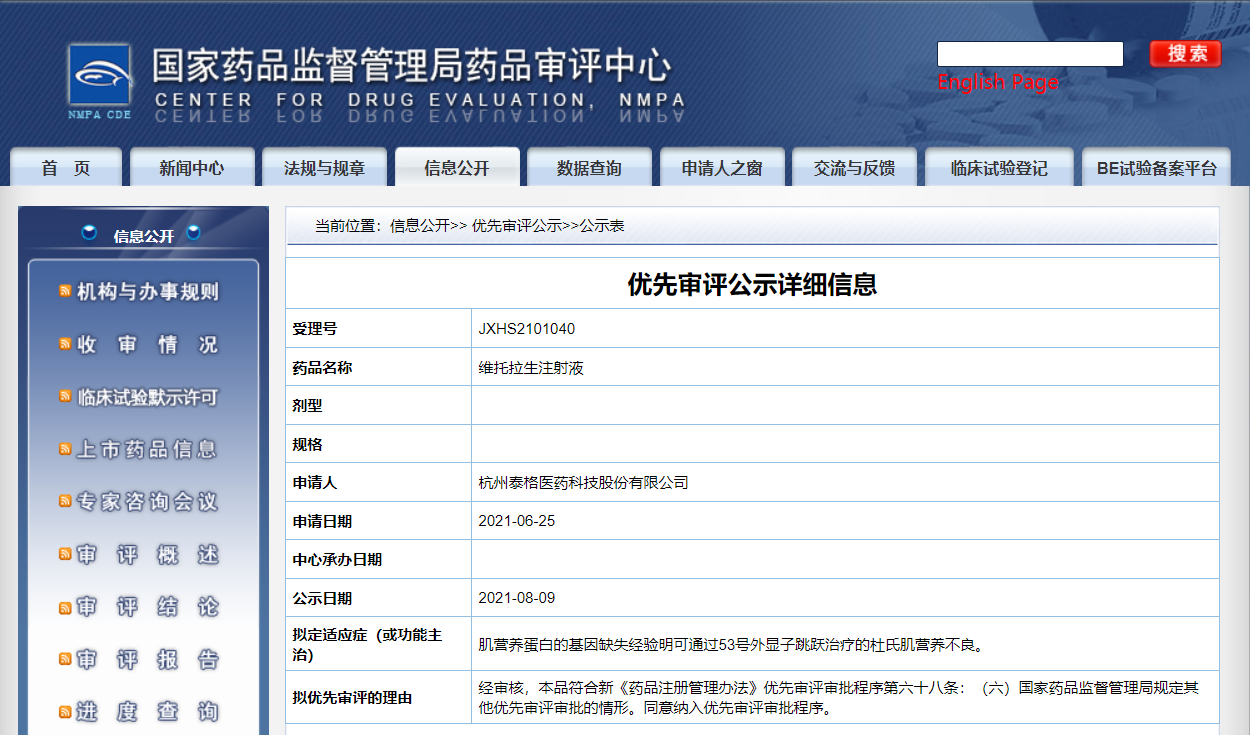
来源:CDE官网
点击查看:
http://www.cde.org.cn/news.do?method=changePage&pageName=service&frameStr=20#


